OLABS ∨
解决方案 ∨

6月22-24日,由 广州市科创委主办的2018中国创新创业成果交易会在广州广交会展馆盛大召开。本届创交会以“双创新动能,引领新跨越”为主题,其展示展览区域超2.1万平米,共规划20多个主题展区,展示创新项目超1000项,并同期开展30多场专项活动(包括主题论坛、路演大赛、项目对接会等),汇聚了超过200位海内外IAB(新一代技术、人工智能、生物医药)、NEM(新能源、新材料)、军民融合、VR/AR等领域嘉宾、20多位院士及100多位风投嘉宾到场,现场可谓是人才济济。其中,奥咨达CDMO+CRO——医疗器械全产业服务平台更是以其专业的法规知识与职业素养,在“2018创新创业成果交易会”上, 展现出了不一样的光芒与专业的气质,吸引了各方,特别是各大投资机构的深度关注!
医疗器械正处于迅猛发展阶段,关系民生民情,高端医疗器械也开始慢慢走入了民众的生活。在人口众多、老龄化问题日益严重的日本,医疗器械已经可以代替护工,照顾退休老人,可见医械发展对提高大众生活水平的重要作用!中国民众也应普及了解医械的发展与其在老龄化社会的关键作用,才能激励产业更好地发展与创新!

奥咨达创交会形象展示
奥咨达为您扫盲!CDMO+CRO?
出现在大众展会的奥咨达,以其专业的企业背景与新颖的创新服务,同样吸引了不少大众的目光。面向服务科研人员、医生与新兴企业的全产业服务平台,很多人不解,什么是CDMO+CRO呢?

投资人咨询医疗器械CDMO平台
要介绍CDMO,首先,我们需要从CRO(Contract Research Organization,合同研究组织)与CRA(Contract Regulatory Affairs Organization,合同注册组织)说起了。
在中国,这两种外包服务已经被大家熟知了。CRO与CRA是一种学术性或商业性的组织,以合同为纽带,以外包的形式承担医药、医械工业在研究开发、注册过程中的一项或多项服务的机构或公司。因其以合同的操作形式进行,明确了合作双方的责任和权利,能够得到法律的有效约束与保护。且确实解决了企业相关人员缺失与经验缺失的问题。CRO与CRA不仅能够消除或降低了新药或新的器械在开发与注册所可能涉及的风险,同时也更符合国际化分工的浪潮。这也是奥咨达专业的领域,奥咨达从2004年创立以来,一直致力于医械临床服务与注册服务,以“临床服务”、“注册服务”、“体系服务”三大服务平台,荣获了三张广东省高新技术产品证书。
在此新兴合作形式的推动下,生物医药工业外包合作形式进一步扩展到了CDMO/CMO领域。CDMO从临床前研究、临床试验到商业化生产阶段与企业的研发、采购、生产等整个供应链体系深度对接,为企业提供创新性的工艺研发及规模化生产服务,以附加值较高的技术输出取代单纯的产能输出。因医药领域事关每个人的生命健康安全,因此我们不能单纯的将CDMO/CMO理解为普通的代加工、贴牌生产,其过程中所需的体系、技术、生产工艺、环境设备、洁净等因素都具有严格的标准和高门槛。能够客户提供 GMP 中间体和定制服务的 CDMO/CMO 企业,其生产体系需要经过包括 FDA在内的政府审查,企业的项目管理、生产、流程优化、安全环保(EHS)和信息安全能力也需要接受各个客户的审计。
简而言之,CDMO+CRO平台就是为医械注册人们提供研发推进、样品生产到注册上市的医疗器械全产业服务平台。
创造全新阶段,共促成果转化对接
在展会上有很多人问到奥咨达,为什么会在创立近15年的2018年,准备做“医疗器械全产业服务平台CDMO+CRO”?

奥咨达张远老师
介绍医械注册人制度
自2017年12月上海《医疗器械注册人制度》颁布以来,医疗器械的黄金发展,正式步入了新的阶段,成为了中国医疗器械产业创新发展的里程碑。在《注册人制度》颁布之前,医疗器械的科研转化,是需要取得生产厂房的“生产许可证”与产品的“注册证”,才能生产出样品进行后续的临床注册等多个步骤。这种制度耗费了人力物力与大量的资金,注册人制度颁布以后,创新企业与注册人可以不必自己去寻找厂房、招聘人力,而只需要持有专利与资金,就可以外包给CDMO+CRO的第三方合作平台,完成从生产注册到临床上市的过程。注册人不必耗费自身心力去实现厂房GMP体系建设与企业的经营管理,而可以专注于更高端技术的研究,为我国医疗领域带来更完善的健康服务,更高端实惠的医疗保障。
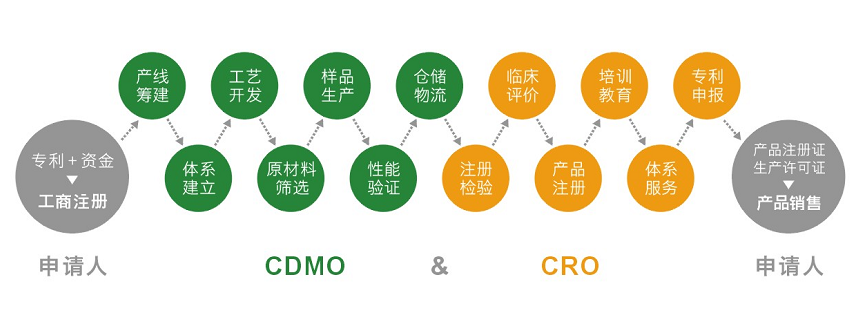
CDMO+CRO平台服务示意图
在政策利好的大前景下,中华人民共和国十九大提出了“健康中国”战略,奥咨达作为高端医疗器械的临床注册专家与全方位、一站式、全产业服务平台的提供方,协助中国医疗水平的提高,是我们不可推卸的责任!随着改革开放以来,研发医疗科研水平也不断提升,但真正用到临床上的技术少之又少。科研成果若不实现科研转化,成为上市产品,又如何服务于国民的医疗需求呢?
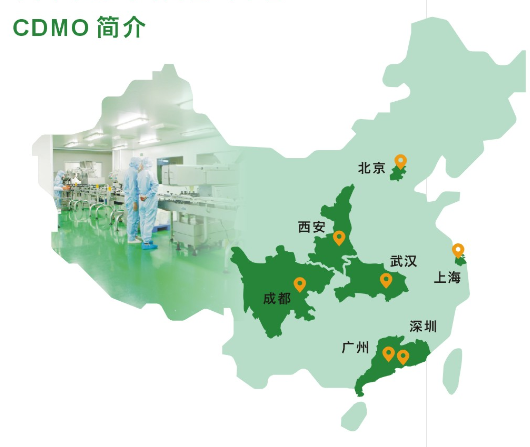
奥咨达CDMO平台规划布局
本次的创新创业成果交易会,与奥咨达医疗器械全产业服务平台CDMO+CRO有着相同的目标:提高科研成果的转化,实现与助力科研学者们成果的落地。随着医疗器械注册人制度试点扩张到广东、天津,奥咨达预计在2018年10月,将医疗器械CDMO平台正式在上海、广州、深圳落地!结合上海注册人制度法规与尚未颁布的广东注册人制度具体实施法规,为医疗器械产业提供创新发展的助力!
奥咨达已在上海、佛山开展了《解读医疗器械注册人制度》的论坛活动,为进一步推进企业的创新发展,奥咨达医疗器械注册人制度解读分享会 (广州站、深圳站)也将陆续开展,奥咨达将为您带来行业新的资讯!感谢您的关注!
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632