OLABS ∨
解决方案 ∨

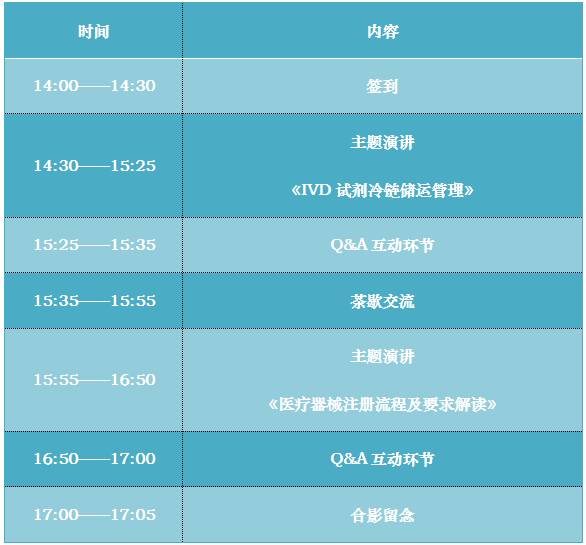
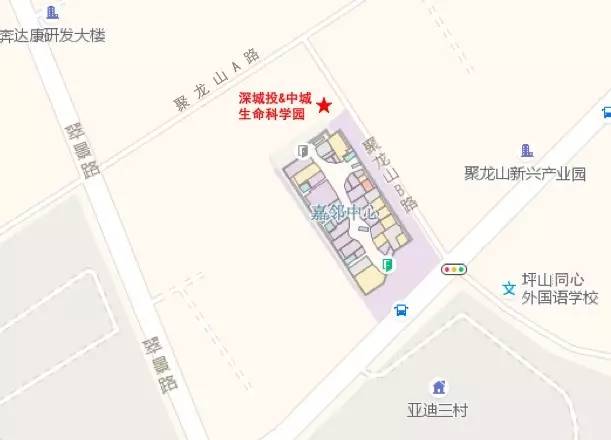
活动导读 很多IVD试剂是生物制品,其生产、运输、储存有严格的条件要求,如需在2℃~8℃下冷藏等。但是,由于目前冷链物流的硬件设施不完备、市场化程度低、运输费用高,IVD试剂发货散、少等原因,并非所有企业都采用冷链车运输IVD试剂,一些企业仍采用泡沫箱加冰袋的包装形式来控制运输过程中的温度条件。然而,这种运输模式无法保证2℃~8℃冷藏的要求,为IVD试剂的质量安全埋下了隐患。 嘉宾介绍 主讲嘉宾一 毛盾 深圳远达创新技术有限公司总经理 毛盾,高级工程师,毕业于暨南大学工程力学系,从事IVD相关产品的包装开发与管理工作10年,先后供职于迈瑞医疗、华为技术,在医药冷链包装、医疗电子设备包装可靠性方面具有丰富的工程经验,主导过迈瑞医疗生化、免疫产品线的包装工作,可以快速有效的推动医疗企业包装可靠性系统建设与包装国际化工作。现任深圳远达创新技术有限公司总经理,远达创新是一站式的冷链温控服务商,专注于中国IVD冷链环境的温控管理与冷链包装技术开发。 演讲主题 IVD试剂冷链储运管理 主讲嘉宾二 王智 奥咨达医疗器械服集团 注册经理 王智,奥咨达医疗器械服集团注册经理;医疗器械注册、法规、体系高级顾问。 擅长领域: 有源医疗器械注册和体系咨询 移动医疗产品、医疗器械软件法规咨询 工作经历: 10余年工作经验,历任有源医疗器械公司软、硬件工程师、项目经理、研发主管,并兼任体系主管。具有丰富的产品开发、注册及质量管理体系经验。 演讲大纲 1.医疗器械注册流程 首次注册流程 首次注册要点说明 延续注册和许可事项变更要点说明 2.如何编写注册申报资料 注册申报资料要求解读 医疗器械软件注册技术审查指导原则要点说明 医疗器械网络安全注册技术审查指导原则要点说明 演讲主题 医疗器械注册流程及要求解读 活动议程 活动费用 公益活动免费,请网上提前报名。 报名方式 点击链接“我要报名”, 时间地点 2017年06月23日 周五下午14:00——17:00 坪山新区聚龙山A路与聚龙山B路交汇处 深城投&中城 生命科学园 1楼报告厅(嘉邻中心停车场入口右手边) 主办单位 主办单位:深圳市坪山区人力资源局 承办单位:深圳伞友临床报告厅 中城新产业控股(深圳)有限公司 活动联系人 王小姐:13528403818
![]()
![]()


![]()
![]()

如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632