OLABS ∨
解决方案 ∨

由于美国国会未能就“边境墙”临时拨款法案达成一致,部分联邦政府机构从2018年12月22日零时起“停摆”,直至2019年1月25日才逐步恢复运行,成为史上最长政府停摆期。据悉在此期间,FDA关闭其部分“非核心”业务,比如FDA只处理威胁人生命安全的紧急事件和重大事件,以及申请人已支付了费用的审评监督工作,暂时停止进行新的工厂检查,也不接受新的注册审核申请。这极大影响相关生产企业的运营。
可见,如果您计划进军海外市场,或已取得海外认证,全面了解海外医疗器械市场监管动态是一堂必修课。
该去哪儿补课呢?
奥咨达蓝皮书系列《2018奥咨达医疗器械行业研究报告》全面介绍2018年美国、欧盟、加拿大、澳大利亚等主要国家以及国际标准化组织(ISO)、国际医疗器械监管者论坛(IMDRF)等国际组织的监管动态与进展。比如:
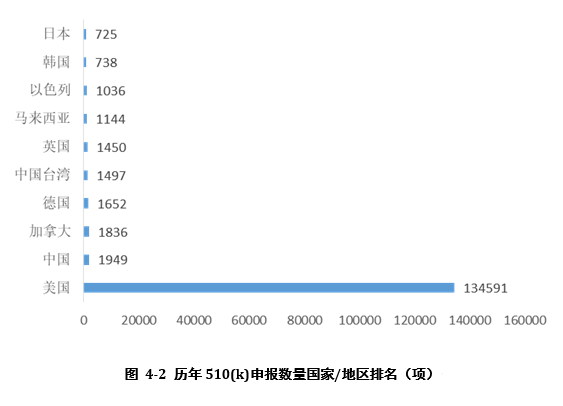
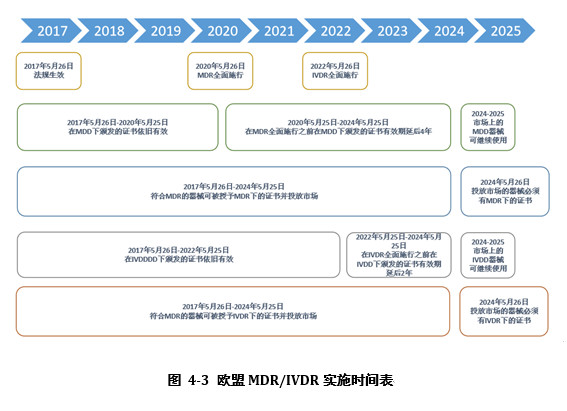
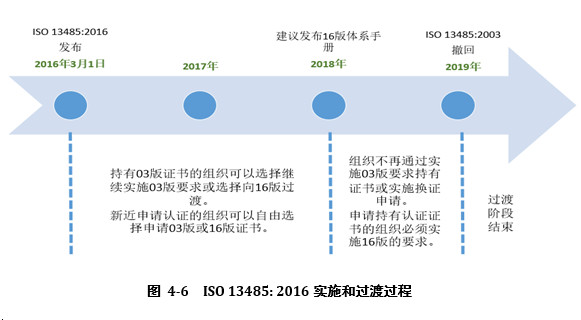
在政策的重大利好下,我国医疗器械逐渐向中高端市场进军,通过持续的研发投入和技术创新,中国医疗器械龙头已积累了部分核心技术,并在某些领域开始突破。未来,在国内外高端医疗器械市场,将会出现越来越多的“中国智造”产品。
如何堂堂正正在国际舞台亮相?答案尽在《2018奥咨达医疗器械行业研究报告》!
2019年4月下旬重磅面世,更多专业内容不容错过,数量有限,欲购从速!

扫描二维码预定
2018奥咨达医疗器械行业研究报告目录
编 委 会
序 言
目 录
概 述
第一章 生产组织方式创新 改变产业发展格局
一.医疗器械上市许可持有人制度的探索
(一)政策发布的背景
(二)政策在上海试点的情况
(三)政策在广东、天津的拓展
(四)政策对产业发展的影响
二.医疗器械3C产业平台,是顺应时代发展的创新模式
(一)医疗器械CDMO的诞生
(二)医疗器械CDMO的价值
(三)奥咨达3C创新平台,一站式闭环服务,填补医疗器械产业空白
(四)奥咨达3C创新平台,实现医工转化新业态,推动产业集聚发展
(五)奥咨达3C创新平台,促进全国各地医疗器械产业均衡发展
(六)奥咨达3C创新平台,构建创新医疗器械产业生态圈
第二章 2018年中国医疗器械法规和监管概览
一.2018年中国医疗器械法规发布概况
二.重点法规及监管事件解析
(一)监管“母法”的修订
(二)产品注册前的相关法规文件
(三)产品注册中的适用法规文件
(四)产品注册后的相关法规
(五)产品上市后的相关规章
(六)任重道远——上市许可持有人制度
三.近年国家局注册审批及创新优先审批情况
(一)2018年国家局注册审评审批情况
(二)2015-2018年国家局注册审评审批情况
(三)国家创新医疗器械审批概况
(四)国家优先审评审批医疗器械情况
四.近年医疗器械注册退审和撤审汇总
(一)2018年国家局不予注册发布情况
(二)2014-2018年国家局不予注册统计
(三)2014-2018年企业主动撤回情况统计
五.2018年国内医疗器械监管动态
(一)境内医疗器械生产企业飞行检查情况
(二)境外医疗器械生产企业飞行检查情况
(三)医疗器械经营质量管理规范飞行检查
(四)医疗器械质量抽检情况
(五)医疗器械召回情况
第三章 中国医疗器械临床评价发展状况
一.临床评价法规监管动态
二.医疗器械临床评价及其常见问题
(一)豁免路径
(二)同品种路径
(三)临床试验
三.体外诊断试剂临床评价的常见问题及展望
(一)体外诊断试剂临床评价的常见问题
(二)体外诊断试剂临床评价的展望
四.临床试验数据管理监管概况
(一)医疗器械临床试验数据管理简况
(二)电子数据采集(EDC)
(三)数据标准化
(四)数据管理的整体趋势
五.医疗器械临床试验生物统计现状和趋势
(一)医疗器械生物统计的作用
(二)生物统计相关指南及其发展
(三)生物统计关键点及现状解析
(四)生物统计学在临床试验应用展望
六.医疗器械临床评价未来发展展望
(一)医疗器械临床评价的几点思考
(二)医疗器械临床评价的未来发展与展望
第四章 2018年国际医疗器械监管动态
一.美国医疗器械监管动态概述
二.欧盟CE认证监管动态
三.其他国家监管动态
(一)加拿大
(二)澳大利亚
四.其他国际组织动态
(一)国际标准化组织,ISO
(二)国际医疗器械监管者论坛,IMDRF
五.专业精准的翻译,助力全球法规监管精要的传播
……
附录
附录1. 2018年国务院发布关于医疗器械的法规文件清单
附录2. 2018年其他部委发布关于医疗器械的法规文件清单
附录3. 2018年国家药监主管部门发布关于医疗器械的法规文件情况
附录4. 2018年国家药品监督管理局发布医疗器械指导原则的通告
附录5. 2018年市场总局、国家药品监督管理局发布医疗器械法规文件征求意见稿
附录6. 2018年发布医疗器械行业标准清单
附录7. 2014年至今国家局创新医疗器械公示产品清单
附录8. 医疗器械临床试验机构备案信息
附录9. 2018年FDA发布指南性文件清单【中英文对照】
附录10. 欧盟施行MDR/IVDR相关重要事项时间安排
附录11. 现行法规欧盟官方公告机构清单

如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632