OLABS ∨
解决方案 ∨
【专家解读】栏目中,奥咨达专家解读之心血管支架(一)在上周发布,各位读者获得的是心血管支架的概述和市场方面的信息。
这一周,奥咨达将分享最全面的可降解支架的在研情况,带您一起看一看国际上知名的雅培、波士顿等企业的研发情况。另外,我们还将带您一同回顾我国国产可降解支架的研发成长历程。
可降解支架是心脏支架发展史上的又一次革命,是一个里程碑式的突破。其功能初期起到支撑作用,然后在体内逐步全部吸收,是恢复血管自身功能理想的转归方式。除了可预防血管的即刻弹性回缩外,携带的抗增殖药物可解决收缩性重塑和内皮增殖,其优势显现于完全吸收后,理想状态表现为恢复血管弹性;晚期的管腔面积增加,减少了晚期贴壁不良;恢复血管的内皮功能;可克服因金属支架内皮化不全所致的晚期和极晚期支架内血栓(stent thrombosis, ST)发生,对再次血运重建(介入或冠状动脉旁路移植术)的策略选择更为重要。
聚合物可降解支架,所用材料包括左旋聚乳酸(PLLA)、聚羟基乙酸/聚乳酸共聚物(PLGA)、聚已内酯(PCL)等,其中左旋聚乳酸(PLLA)和聚羟基乙酸/聚乳酸共聚物(PLGA)已被美国FDA批准为植入人体的生物工程材料。
目前此类材料的主要研究者为:美国雅培公司(Absorb BVS 支架)、美国Reva Medical公司(Reva和ReZolve支架)、日本KyotoMedical公司(Igaki-Tamai支架)、北京乐普医疗(NeoVas支架)、山东华安(Xinsorb 支架)和上海微创医疗(Firesorb 支架)。
国外品牌
1、美国雅培
Absorb是全世界首个能完全被人体吸收的血管支架,由雅培公司生产,于2011年和2016年在欧洲和美国上市。Absorb目前已经在全球100多个国家上市使用,并在全球用于150,000人的治疗。
Absorb BVS是首个进行临床实验的药物洗脱完全生物可降解血管支架,成为在全世界首个并且唯一上市的全吸收式生物血管支架。该支架的材料是左旋聚乳酸(PLLA),表面涂覆上 PDLLA 涂层,厚度为160μm,含有抗增殖药物依维莫司,载药浓度为8.2μg/mm,完全降解需要3年时间。该产品的上市对冠状动脉疾病的治疗具有划时代的意义[4]。
2015年的Absorb系列临床试验中3,389例患者的荟萃分析结果表明,Absorb安全性较好,可与目前被广泛认可的金属药物洗脱支架Xience CoCr-EES(钴铬合金依维莫司洗脱支架)相媲美。在全球范围内进行的Absorb的系列临床试验主要包括AbsorbⅡ(欧洲)、Absorb Ⅲ(美国)、Absorb Japan(日本)、Absorb China(中国),其试验结果一直受到广泛关注。
2017年公布的Absorb Ⅲ的2年期临床试验结果:在2.25mm 直径以上的病变血管适应症范围内,Absorb 的安全性无疑。但Absorb靶病变失败风险及靶血管心肌梗死事件明显高于药物洗脱支架,引发了公众对Absorb支架的前景产生了怀疑。此后,美国FDA于3月18日发布公告,警示Absorb可增加严重心脏不良事件风险,提醒医生严格依照适应症植入Absorb,不得在小血管中植入。紧接着的3月31日,欧盟监管当局宣布:从5月31日起Absorb WT1生物可吸收支架不能在欧洲广泛地使用[5]。
在2017年9月8日雅培突然以销售不理想为由停止了这款产品的上市,并在10月23日向原NMPA国家局申请:主动撤回正在评审的医疗器械注册申请“全吸收式生物血管支架系统”(受理号JQZ1600457)。
不过,就在雅培退市的同期、2017年5月召开的EuroPCR大会上,我国心血管病专家高润霖院士公布了Absorb China三年的临床结果,Absorb在置入患者体内三年内,靶病变失败率和支架内血栓发生率这两项指标与Xience V支架相似:Absorb靶病变失败率和支架内血栓发生率均与药物洗脱支架无差异,在2-3年间,两款支架均未发生支架内血栓。Absorb China三年期的临床试验结果喜人,再次证明了可降解支架的在适应症范围内的安全性。这得益于我国每年的冠脉植入手术量较大,大医院的冠脉植入经验丰富,可降解支架适应症选择和控制手术风险中更具经验。
此外,AbsorbJapan的研究结果也较为理想,Absorb在2-3年间仅1例发生支架内血栓,总体时间发生率仅为1.6%,与金属支架无差异。
高润霖院士指出,Absorb China和Absorb Japan临床试验结果较好的原因是选择了合适大小的血管(直径大于2.25mm),并严格遵守PSP原则,即充分的预扩张和完全后扩张。
2、日本KyotoMedical
Igaki-Tamai支架,是最早应用于人体的可降解支架。1998年日本的Kyoto Medical公司研制生产出第一个没有药物涂层的聚乳酸BRS,完全吸收需要约18~24个月。BRS 的这种暂时存留性特点与血管再狭窄的时间相吻合,其在血管内皮化完成后开始降解,保持了血管结构的完整并稳定了血管的内环境。
经过10年随访,随访结果显示支架完全被吸收,死亡病例并不高,其心源性死亡率为2.2%。与金属支架相比,Igaki-Tamai支架并不引起更显著的内膜增生,具有良好的组织相容性,在欧洲批准用于下肢血管支架手术使用。
3、美国RevaMedical公司
美国RevaMedical公司设计研发的第一代络氨酸聚碳酸酯(tyrosine polycarbonate)可吸收支架(Fantom支架),在体内可降解为水、二氧化碳、乙醇及碘化酪氨酸烷基等,降解产物对人体几乎无毒副作用,均可被人体吸收或排出体外。该支架厚度达228 μm,采用独特的“滑动和锁定”设计,能在支架置入后提供足够强的径向支撑力,且支架注入不透射线的碘来做标记物,有助于后期随访。
Reva支架是一种球囊扩张支架,充分扩张后可覆盖动脉壁的55%。Pollman等初次应用于人体的临床试验报道了该支架的高临床事件发生率:TLR 67%。这主要是由于支架在血管内扩张不充分所致。
后来,Reva公司重新设计了第二代可吸收支架ReZolve,该支架采用了重新设计的“螺旋滑锁”结构,并包含西罗莫司药物涂层,支架厚度114 μm;Restonne研究旨在评价该支架的安全性及有效性,纳入50例患者,目前实验正在进行中;研究一级终点是6个月TLR率及12个月冠状动脉定量分析(QCA及IVUS)。第二代的支架提高了药物剂量,并具有更慢的药物释放系统。
4、波士顿科学
从目前的研发状况来看,可降解支架基本是在成熟的药物洗脱支架基础上研发而来,主体在于材质创新。值得注意的是,可降解PLA路线本身有诸多问题。从长期效应来看,金属支架残留最主要的问题是影响血管术后正常收缩。
在国际上,波士顿科学的Synergy支架系统就采用了与雅培不同的实施路线。Synergy于2012年在欧洲获批上市,稍早于Absorb于2015年10月在美国获批。与Absorb的研发路径类似的是,Synergy亦大幅沿用了波士顿科学前代DES产品PROMUS Element的相关工艺,包括结构和缓释药物。
与Absorb的完全吸收不同,Synergy最终残留较薄的金属支架,可称之为不完全可降解支架。Synergy的金属支架部分最终会被内皮化的血管内壁细胞所包裹,减少支架对患处的刺激,从而规避支架内血栓的形成。相对Absorb而言,Synergy更为传统,关注的是一直作为研发焦点的表面处理工艺,选择了对表面涂层模式和药物释放时间控制进行创新而非彻底改变支架状态。
Synergy在结构上同样沿用了波士顿科学自身早先的PROMUS系列的金属底架的基本结构,以极薄(74μm)的铂铬合金作为结构基础,使用比一般涂层更薄(4μm)的可降解PLA作为药物释放涂层,替换PROMUS 系列的表面聚合物涂层置于合金骨架表面(与血管壁接触的管腔面)。
Synergy的PLA涂层在安装后3个月的时间即基本降解完毕,这一降解速度高于目前同类产品,同时随聚合物降解可有效释放洗脱药物,减少对内皮组织的不当刺激。这些特点都显示了Synergy立足于血管内皮化的研发导向。
国产品牌
与雅培和波士顿科学的分歧相应,国内企业研发路径也主要有两种:以乐普医疗为代表的技术研发型企业追随雅培,借助自身已有的成熟DES工艺和结构,以PLA可降解材料和完全可降解支架为主要研发方向;以上海微创为代表的另一种工艺研发型企业选择在现有药物洗脱支架的基础上进行进一步研发改造,改善表面处理、药物释放或其他工艺,提升内皮化效果[6]。
国内有多家企业正在如火如荼地进行完全可降解支架的研发和开展临床验证,不断传出令人振奋的消息:
2013年,中科院院士葛均波教授与华安生物合作成功研发出了新一代完全可降解支架“生物全降解冠脉雷帕霉素洗脱支架系统(Xinsorb)”,并且率先完成了国内首例完全可降解支架(BVS)植入手术。该产品已开始了确诊性临床试验,于2017年CIT会议期间公布的初步数据验证其安全有效性。
2016年1月,微创医疗“生物可吸收雷帕霉素靶向洗脱冠脉支架系统(Firesorb)”于中国医学科学院阜外医院完成了首例入组,并在2016年TCT大会和2017年CIT大会上分别公布了6个月及12个月的造影结果,充分证实了该产品具有良好的临床初步应用安全性和有效性。后续将于2017年8月、2018年第二季度开展Ⅱ、Ⅲ期临床试验。
2016年9月,北京阿迈特“可吸收冠脉血管支架(AMSorb)”作为世界上唯一一家利用3D精密打印技术生产的多聚物可吸收支架的临床试验FIM,也由北大第一医院霍勇主任牵头启动了,目前正在筹备RCT阶段。
2017年8月,乐普医疗的 “全降解聚合物基体药物(雷帕霉素)洗脱支架系统(NeoVas)”得到国家局的医疗器械注册受理(受理号:CQZ1700369),并按照《创新医疗器械特别审批程序(试行)》进行注册审批,予以优先办理。在今年CIT大会上,韩雅玲院士报告了NeoVas生物可吸收支架的多中心随机对照试验一年随访结果:晚期管腔丢失无差异、支架覆盖率更高、支架贴壁不良率更低。
更令国人为之自豪的是,2018年9月4日,世界顶级权威医学杂志《柳叶刀》全文刊登了微创医疗自主研发的Firehawk(火鹰)冠脉雷帕霉素靶向洗脱支架系统在欧洲大规模临床试验(TARGETAC)的研究结果,这是《柳叶刀》创刊近200年来首次出现中国医疗器械的身影。根据试验结果,火鹰作为第三代靶向药物洗脱支架,在植入患者体内后,受到治疗的血管区域能够在早期快速愈合,因为其创新性的微槽包裹药物、生物可降解聚合物的设计,以及较低的载药量(仅需同类产品三分之一的载药量即可实现同等疗效),即证实了Firehawk支架对Xience支架的非劣性。而对于长期安全性和有效性,上海微创也做出相关说明:需要PCI手术后5年进行随访研究[7]。
但无论如何,对金属支架的600个凹槽确实证实了其非劣性。换而言之,支架安全性和有效性的提高除了进一步发展成全降解支架这一个方向以外,还有可以依靠进一步改良已经成熟的第三代金属支架技术来实现。
另外,有资料显示:截止去年10月,国内一共有3个支架进入临床,而且已经有2个已经完成了全部的临床试验1230例,至少还有7家企业还在研究这种支架,他们其中的9个产品进入了国家局的创新产品审批通道:
表3-1 进入创新医疗器械审批通道的支架系统
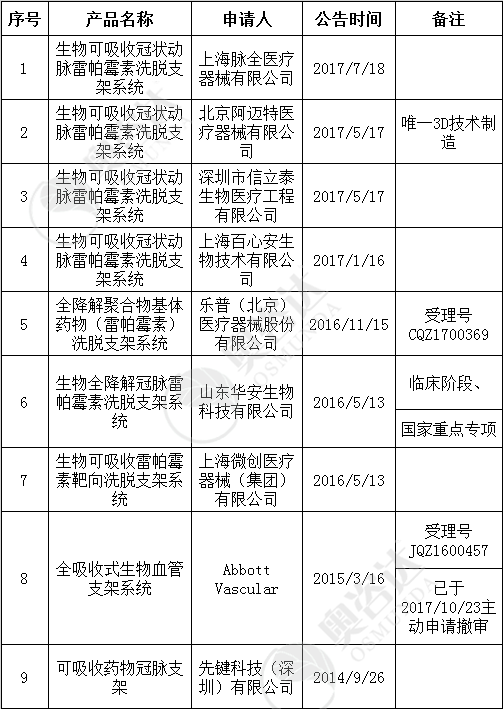
资料来源:NMPA官网,奥咨达整理
下面简单介绍一下同类产中品进展较快的国内代表:
1、乐普医疗
乐普医疗与沈阳军区总医院韩雅玲院士团队合作研发的是全降解聚合物基体药物(雷帕霉素)洗脱支架系统(NeoVas),它以PLLA为平台,PDLLA为支架涂层,含有雷帕霉素(15.3μg/mm)[8]。
NeoVas临床结果表明,与CoCr-EES药物洗脱支架对照组相比,靶病变失败、患者驱使的不良事件、全因死亡、靶血管心肌梗死、血运重建、卒中及支架内血栓形成等指标无显著差异,说明NeoVas的主要重点及临床结局均具有非劣性。
研究表明,就主要终点而言,随访一年后NeoVas RCT研究和Register研究的TLF率达到了目标值,且包括PoCE、所有原因的死亡率、心源性死亡等在内的疾病发生率相对较低。综上,NeoVas首次人体临床试验取得了令人满意的结果。
NeoVas已处于注册审评发补阶段,而其他同类产品均处于临床试验或之前阶段。随着雅培2017年10月的主动撤回正在审评中的医疗器械注册申请,乐普医疗的NeoVas有望成为全降解药物支架产品的第一张国内上市通行证。
2、山东华安
山东华安的Xinsorb支架,是首个由国内企业自主研发的完全可降解PLA 支架。该支架由PLLA构成,支架表面涂覆含有抗增殖药物雷帕霉素的PDLLA涂层。支架采用球囊扩张方式释放,支架两端各有1个不透X线的标记,用于指示支架在血管中的位置。支架厚度为160μm,载药量8 μg/mm,体外测试显示80%的药物在28 天内洗脱。
复旦大学附属中山医院葛均波院士于2013年9月5日率先成功完成我国首例由国人自主研发的完全可降解聚乳酸支架的植入。Xinsorb支架与Excel支架的对比动物实验结果显示,短期内冠脉狭窄无显著差异。长期的有效性及安全性有待进一步研究。2014 年7月,Xinsorb 生物可吸收支架进入随机对照临床试验阶段。2017 年3月CIT会议的最新结果显示,Xinsorb支架的临床结果表明,与Tivoli药物洗脱金属支架对照组相比,Xinsorb具有减少患者驱使的不良事件、靶病变失败和缺血驱动的靶病变血运重建的趋势,对于高度选择性患者,Xinsorb具有和Tivoli金属支架相似的安全性和有效性。
3、微创医疗
微创医疗的Firesorb生物可降解支架是以可体内降解的高分子材料聚左旋乳酸(PLLA)为骨架材料,是第二代可降解药物洗脱支架,具有支架厚度较薄的特点。以聚D,L-丙交酯 (PDLLA)为表层材料的厚度仅为100-125μm,比雅培的Absorb的140-150μm还薄,是目前临床上最薄的可降解药物洗脱支架之一,以低剂量的西罗莫司作为洗脱药物。现已进入临床试验的第二阶段。
Firehawk冠脉雷帕霉素靶向洗脱支架系统(Target ElutingStent,TES)也采取了这一路线。Firehawk被公司称为“全球第一及唯一的靶向洗脱支架系统”,主要思路是减少药物涂层面积和药物总量,平均金属覆盖率14.0-16.1%。公司称该支架为全球最低载药量支架,通过“同类产品1/3载药量获得相同的 有效性”。在结构上与Excel、Synergy相似,通过金属支架血管壁侧定向凹槽,借助3D打印进行药物填充,以控制药物释放、减少载药和聚合物装量,加速血管内皮化。
特别地,目前火鹰支架的药剂量为全球最低。其使用者服用双重抗血小板药物的时间预期可以从长期治疗缩短至1个月,可为患者每人每年节省近万元,如果服用其他新型抗血小板凝聚药物则节省更多,可为国家医保每年节省支出近60亿元。
此外,更为稳定的药物释放工艺、血管壁侧金属支架纳米处理、金属支架直接连接释放药物去除有不良影响的高分子层等等研发路径均有国内支架生产企业予以研发,以血管更快内皮化为导向的产品在临床上也有不俗的表现。
表3-2 国内主要在研的同类产品对比
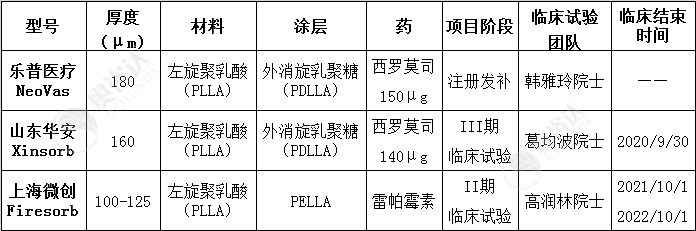
资料来源:公开资料整理
以Absorb、乐普和Synergy、微创为代表的全降解和金属结构支撑加强表面处理两大主流方向各有优劣,更新研发仍在展开。从现有技术发展和临床效果来看,PLA全降解不能完全解决相关问题。未来更新换代的全降解支架和金属基础支架谁将最终胜出,仍要靠临床和市场检验。
表3-3 目前国内外在研的主要同类产品对比
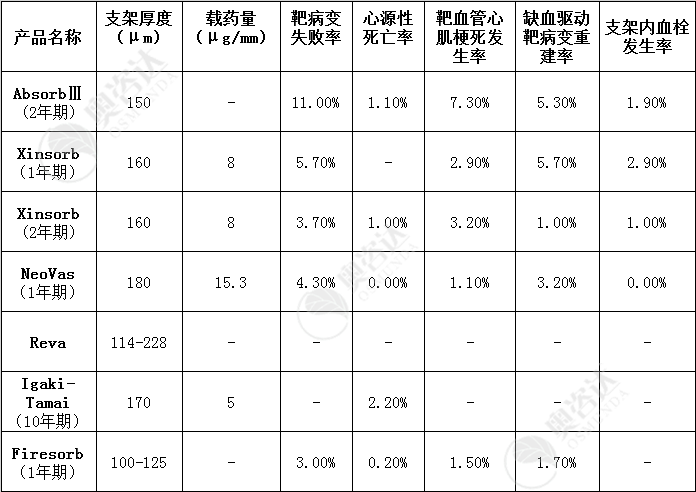
资料来源:公开资料整理
更多精彩内容,敬请期待下一期的【专家解读】
奥咨达的专家还撰写了
2018年奥咨达
医疗器械行业蓝皮书
将于2019年给您一个完美的开门红!

参考文献
[4] 高立建,盘点:生物可吸收支架的研发应用进展[EB/OL].http://news.medlive.cn/heart/info-progress/show-138600_129.html
[5] 奚廷斐,全降解药物洗脱支架进展及挑战,[EB/OL].http://drug.39.net/xwsd/170906/5678579.html
[6] OCC2017创新 | 葛均波:生物可吸收支架,中国的!PCI革命![EB/OL].http://www.sohu.com/a/144040722_688893
[7] Lansky A, Wijns W,Xu B, et al. Targeted therapy with a localised abluminal groove, low-dosesirolimus-eluting, biodegradable polymer coronary stent (TARGET All Comers): amulticentre, open-label, randomised non-inferiority trial[J]. Lancet, 2018.
[8] ESC 2017|中国证据:韩雅玲院士公布NeoVas用于冠状动脉病变患者的效果随机对照研究结果[EB/OL].https://www.sohu.com/a/168222065_186367
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632