OLABS ∨
解决方案 ∨
ART医疗器械注册情况和法规监管动态
人类辅助生殖技术(Assisted Reproductive Technology,ART)在我国大陆地区发展28年,近15年来,该项技术迅速成长,随着相关技术、服务在国内的普及和深入,现临床上涌现出越来越多的ART用医疗器械,并呈飞速增长。
ART用医疗器械品种多而杂,不孕不育症患者在使用ART相关医疗器械的同时也面临着风险,临床医师或胚胎学家需采用相关的一系列医疗器械进行的辅助生殖体外诊疗,这关系到患者自身的安全和最终的临床结局。为此,需要相关的法规指南和管理规范,来引导和规范我国ART用医疗器械注册上市,并保证其安全可靠、合理规范,从而进一步提高辅助生殖技术服务。鉴于此,本文就ART相关医疗器械注册上市现状及其监管的法规动态来进行阐述。
一、ART医疗器械上市注册情况
截至2018年10月31日,分别以“胚胎”、“囊胚”、“配子”、“合子”、“精子”、“卵”等关键词搜索国家药品监督管理局的医疗器械数据库筛选并统计结果。以“胚胎”为关键词查找出有35个进口器械和8个国产器械取得注册证;以“囊胚”为关键词查找出有10个进口器械取得注册证,但无相关国产器械注册信息;以“配子”为关键词查找出有4个进口医疗器械取得注册证,同样无相关的国产器械注册信息;以“精子”为关键词查找出有33个进口器械和45个国产器械取得注册证;以“卵”为关键词查找,排除体外诊断试剂盒,共有33个进口器械和12个国产器械取得注册证;以“合子”为关键词查找,未搜索到相关进口和国产ART医疗器械的注册信息。
从以上注册信息看出,取得注册证的国产操作类产品主要是作为Ⅰ类医疗器械注册的精子采样管和作为Ⅱ类医疗器械注册的一次性使用无菌取卵针、单腔/双腔取卵针、胚胎活检针、卵母细胞采集器和胚胎移植导管类产品。取得注册证的国产液体类产品主要为Ⅰ类医疗器械备案的精液洗涤液和回收保存精子的液体类产品。
而取得注册证的进口操作类产品除包括以上国产已注册的医疗器械外,还有Ⅱ类医疗器械注册上市的体外受精显微操作管、人工授精导管、ICSI相关穿刺固定针、玻化冻存管等。此外,取得注册证的进口液体类产品均为Ⅲ类医疗器械,该类注册上市的医疗器械包含ART实验室操作流程中所用到的各类液体,如卵泡冲洗液、取卵胚胎处理液、配子缓冲液、洗精授精液、精子显微操作液、卵裂胚培养液、囊胚培养液、胚胎移植培养液、胚胎冷冻保存液等。但截止到目前为止尚未有国产的液体类产品如冷冻保存、复苏液和培养液取得注册证。
胚胎/囊胚的培养、冷冻及复苏是ART常规技术之一,胚胎/囊胚培养液是辅助生殖体外培养阶段配子受精期培养的产品,能为胚胎外发育提供必需的营养物质,通常卵裂期胚胎在培养液中培养2-3天后,可被移植到子宫或继续在体外用囊胚培养液进行3-4天的培养。而胚胎/囊胚的冷冻保存液和复苏液是用于体外辅助生殖技术中各阶段胚胎、卵子及囊胚的冷冻复苏的产品,冷冻保存液和复苏液是首先利用冷冻液将胚胎/囊胚保存在超低温环境中,复苏液则是当需要时再将胚胎/囊胚进行解冻复苏。而这两大类产品基本被国外产品所垄断,国产医疗器械在这一领域基本为空白,因此,如果有国产的胚胎/囊胚培养液和冷冻保存、复苏液注册上市,就辅助生殖技术而言,给患者带来获益同时,简化流通程序,节省操作成本并减轻患者的经济负担具有重要的意义。
二、ART产品法规监管动态
1、美国对ART用医疗器械的监管:
在美国联邦法规(CFR)的21章中第884部分的G项明确规定了ART用医疗器械的分类和定义,ART用医疗器械中的大多数产品被归为Ⅱ类医疗器械进行管理,并针对不同类别的产品(如操作类产品、胚胎/囊胚培养液类产品等)提出了标准化的技术要求(如鼠胚试验、内毒素检测、无菌及生物相容性等)。在CFR中,由于辅助生殖技术的专业特点,ART相关医疗器械(SubpartG-Assisted Reproduction Devices )被归在妇产科器械(Obstetrical And Gynecological Devices)中,与计划生育器械(SubpartF-Obstetrical And Gynecological Therapeutic Devices)等其他的器械分开管理,并有其相关的指导原则进行要求(FDAGuidance:Devices Used for In Vitro Fertlization and Related AssistedReproduction Procedures)。
2、我国对ART用医疗器械的监管:
由于在为不孕不育患者实施辅助生殖技术治疗中,临床医师或胚胎学家需采用相关的一系列医疗器械进行的人类配子/合子和胚胎操作,这关系到患者自身的安全和最终的临床结局。为此,我国根据国情需要,各监管部门制定了相关的法规要求,来规范ART用医疗器械,为保障患者用械安全发挥重大作用。
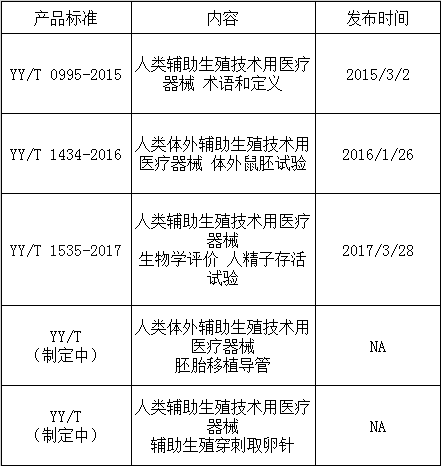
国家药品监督管理局自2016年出台《人类体外辅助生殖技术用液注册技术审查指导原则(征求意见稿)》以来,截至2018年10月31日,相继出台了《人类体外辅助生殖技术用液注册技术审查指导原则》、《辅助生殖用穿刺取卵针产品注册技术审查指导原则(征求意见稿)》、《辅助生殖用胚胎移植导管产品注册技术审查指导原则(征求意见稿)》。见下表所示:

另一方面,国家药品监督管理局自2015年首次针对ART用医疗器械,拟定了人类辅助生殖技术中的体外受精-胚胎移植技术及其衍生技术所使用的医疗器械的术语和定义,后陆续完善制定了一系列相关的辅助生殖技术用医疗器械的标准化内容,相关标准的制定对辅助生殖类医疗器械的研发、生产、技术审评和监管带来了检测方法和标准依据,可作为不孕不育患者进行辅助生殖治疗医疗器械的上市注册的指导性文件。具体如下表所示(截至2018年10月31日):
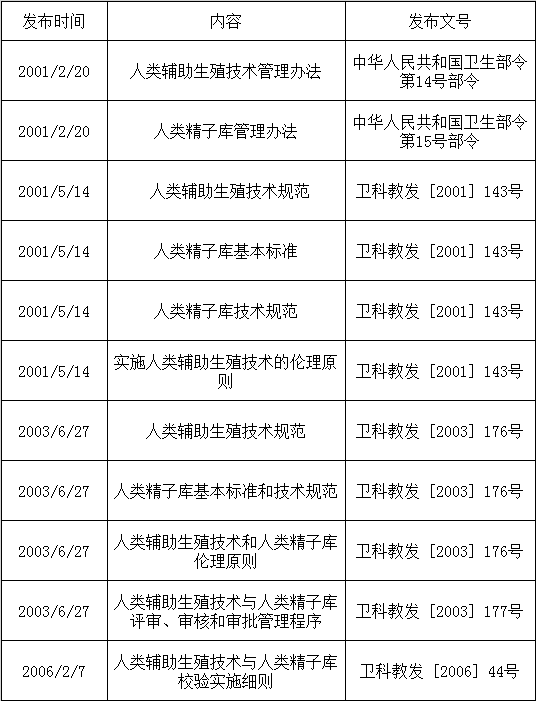
卫生主管部门颁布了一系列针对辅助生育技术的技术规范和管理办法,使得该项技术逐步规范化。为了辅助生育技术的健康发展和良好运行,自2001年起卫生部相继出台《人类辅助生殖技术管理办法》、《人类精子库管理办法》和《人类精子库基本标准和技术规范》。此后随着国内外人类辅助生殖技术、人类精子库技术和生命伦理学的不断进步与发展,卫生部又针对相关法规进行了修改、补充和完善,使其更符合辅助生育技术发展的要求,并且进一步规范了该技术的临床应用。如下表所示:
指导性文件:
1. 国家药品监督管理局医疗器械技术审评中心《指导原则》;
2. 国家药品监督管理局《中华人民共和国医药行业标准》;
3. 中华人民共和国卫生部通告。
参考文献:
章娜,徐丽明,人类辅助生殖技术用医疗器械的监管和标准现状,生殖医学杂志,2015,7:591-595.
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632