OLABS ∨
解决方案 ∨

奥咨达携手深圳市银星集团、深圳前海德盈投资有限公司建立的医疗器械3C(CDMO+CRO+CSO)平台迎合粤港澳大湾区医疗器械发展浪潮, 9月20日将在深圳银星产业园盛大开业运营。平台为医疗器械创新创业、投资机构、医疗器械生产企业、经营企业、科研院校、海外政府与政府机构等医疗器械产业群体提供定制化服务,将以产品服务为基础,从研发转化、器械制造、注册、产业服务、产业基金、医械云扩展至医疗器械上下游产业链,构建创新孵化、产业集聚和资本助力的医疗器械产业生态系统服务,助力大湾区内医疗器械产业战略升级。
开幕仪式将于9月20日,在银星科技大厦一楼大厅盛大展开,诚邀您的莅临与指导!请您查收庆典活动【邀请函】!

自医疗器械注册人制度落地以来,奥咨达秉承推进医疗器械创新成果落地的愿景,打造了医疗器械3C创新服务平台,致力于为医疗器械的创新成果提供更便利、更有效的落地方案。为中国医疗器械产业提供资本聚集、法规聚集、技术聚集、产业聚集与产业加速的医疗器械一站式解决方案。

医疗器械合同研发生产组织(Contract Development Manufacture Organization,CDMO),即医疗器械CDMO平台,是一种新兴外包服务模式,主要接受医疗器械注册申请人的委托,为其提供生产工艺的的开发和改进服务以及临床试验和商业化销售所用原辅料、管理、生产的生产供应服务。CDMO平台可实现从临床前研究、临床试验到商业化生产阶段同医疗器械企业的研发、采购、生产等整个供应链体系深度对接,以取代以往单纯的产能输出,为医疗器械企业提供创新性的工艺研发及规模化生产服务及附加值较高的技术输出。同时,CDMO平台也具备定制研发和生产的能力,有利于创新产品商业化。
从整个医疗器械生命周期看,CDMO服务涉及医疗器械研发设计、产线筹建、体系建立、工艺开发、原材料筛选、样品生产、性能验证、仓储物流等阶段,特别是产品准许进行生产制造后,通常会为CDMO带来大额效益。CDMO核心在于“D”,即“Development”。 从研发、战略思维,到团队、背景成本等方方面面,每一个环节都有法规量化,从原料开始进行改进优化,甚至是创造性的改变。
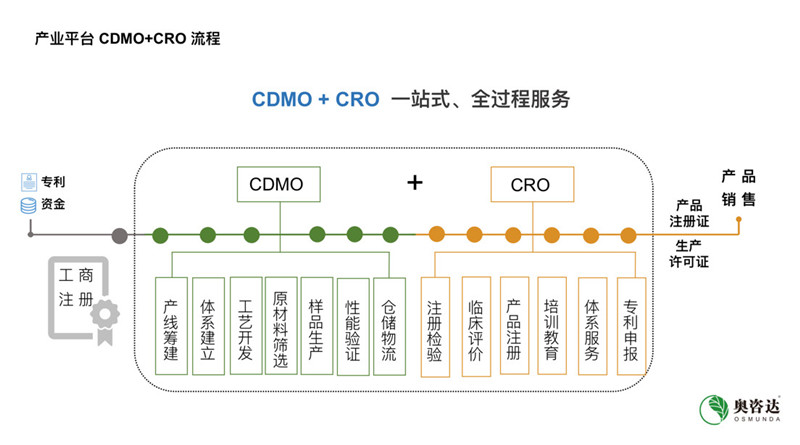
为更好地解决医械成果转化难题,奥咨达联合CDMO+CRO+CSO,致力于建设医疗器械3C创新服务平台,实现更加完善与有效的一站式服务方案,实现缩短产品上市时间、减少企业经营成本、共享经济、合法合规、配套孵化的平台价值。让医疗器械企业真正享受到注册人制度带来的500亿分红!
现在的医械产业政策背景:2018年5月24日,国务院印发《进一步深化中国(广东)自由贸易试验区改革开放方案》和《进一步深化中国(天津)自由贸易试验区改革开放方案》,试点范围进一步扩大。9月5日,关于征求《广东省医疗器械注册人生产质量管理体系实施指南(草案)》的通知颁布。利好政策频频出台,医械中高端创新服务逐步走向规范化、国际对标化,奥咨达将全力推动医疗器械3C创新服务平台的全国性布局,深圳3C创新服务平台的落地将是其关键的第一步。奥咨达特邀各位行业精英来见证与监督,奥咨达将不忘初心——致力于中国成为医疗器械产业聚集中心。
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632