OLABS ∨
解决方案 ∨
为了加快发展佛山高新区的医疗器械战略性新兴产业,适应国家药监部门从严监管的发展态势,鼓励区内医疗器械生产企业规范从事生产经营工作,佛山高新区携手奥咨达高级研修中心正式开启2018年第一期医疗器械法规事务人才培训课程。
为了确保课程的顺利展开,佛山高新区近期对佛山市部分企业(凯洋、大洋、东方、其右、百合)进行走访,充分了解企业需求。

广东凯洋医疗科技集团有限公司

广东大洋医疗科技股份有限公司

佛山其右医疗科技有限公司
培训地点:广东(南海)生物医药产业基地B座一楼展厅会议室
培训内容及时间 培训分理论课程及企业走访辅导两部分,理论课程将围绕GMP法规和质量管理体系等方面开展,课程安排如下: <<<< 滑动可以看到更多内容 自《关于开展佛山高新区2018年第一期医疗器械法规事务人才培训课程的公告》发布日至2018年7月25日,经筛选拟入选企业名单如下: 组织单位 指导单位 佛山国家高新区 广州市生物产业联盟 广东食品药品职业学院 奥咨达医疗器械服务集团 医疗器械临床转化产业联盟 全国卫生产业企业管理协会医疗器械商业分会 中国医疗器械协会中医医疗器械专业委员会 广州市中科医创医疗器械转化医学研究院 主办单位 奥咨达高级研修中心 协办单位 贝壳社 联众医药网 百川医汇创新学院 众享谷(武汉)生物科技有限公司 上海枫林生命健康产业发展(集团)有限公司 课程咨询及合作 全女士 电话:020-62316262-620/13512789186 邮箱:hongxin.quan@osmundacn.com
理论课程培训开始时间为2018年8月6日,共培训11日。企业走访辅导时间为理论课程结束后一个月内。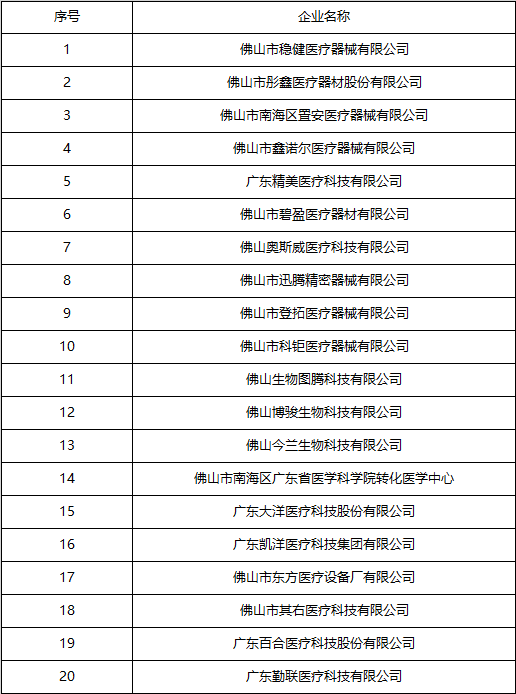
枫林国际创新中心
武汉万竹信息技术有限公司
广药白云山医疗器械创新产业园
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632