OLABS ∨
解决方案 ∨
法规专刊创刊半年以来,以海量的资源和独特的视角,获得了界内好评。
在这快速发展的时代,知识轻量化已成时代潮流。
紧跟时代的步伐,在这多姿多彩的2018年夏季,奥咨达将以更深入的解析,将“成册”的法规专刊,一一做成原创性文章,让广大读者学习到法规知识的同时,没有阅读疲劳,使得时间利用率更高!
以下是法规专刊中临床抽查的内容:
国家药品监督管理总局于2018年6月1日发布了公开征求《医疗器械临床试验检查要点及判定原则(征求意见稿)》意见的通知,征求意见稿根据《医疗器械监督管理条例》《医疗器械注册管理办法》《体外诊断试剂注册管理办法》《医疗器械临床试验质量管理规范》《体外诊断试剂临床试验技术指导原则》等相关要求制订。
另外,国家药品监督管理总局于2018年6月25日发布了2018年第一批医疗器械临床试验监督抽查项目名单(国药监【2018】48号通告)。本次抽查的10个项目中9个为医疗器械临床试验,1个是体外诊断试剂临床试验;进口注册2项,其余均为国内注册项目。
对临床试验进行监督抽查,俨然已成为药监主管部门的常态化工作。本期法规专刊,奥咨达专家给大家回顾一下自2016年以来国家局发布的历次抽查情况。
历史回顾1:2016年至2018年抽查数据一览表
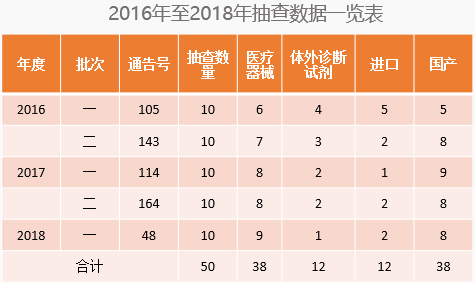
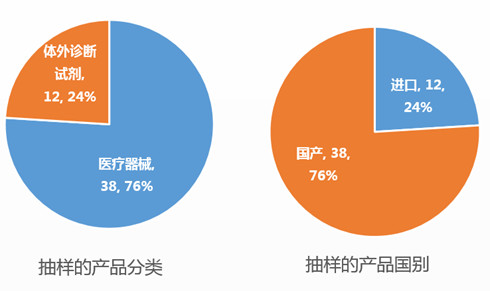
药监局已公布的5个批次抽查项目合计50项,体外诊断试剂项目12项,剩余38项均为医疗器械;进口注册共12项,其余为国产注册,共38项。国产的医疗器械项目占绝大多数。
历史回顾2:已公布结果的2016年至2017年抽查情况汇总
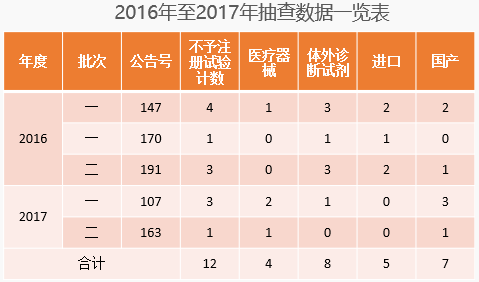
国家局至今公布的5个批次抽查项目合计50项:
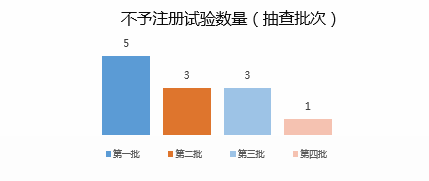
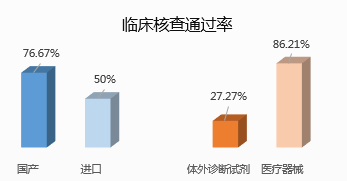
从已公布的检查结果来看,体外诊断试剂是重灾区,在药监局抽查的11项临床试验中仅3项通过检查,占了检查后不予注册的12个项目的三分之二;而进口和国内注册不予注册的数量相差不大(5:7)。
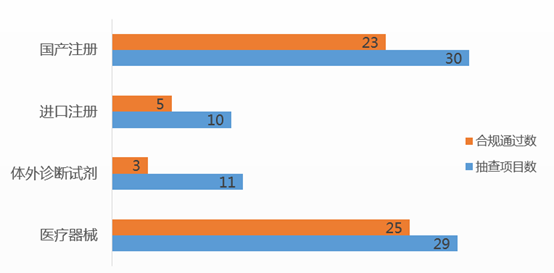
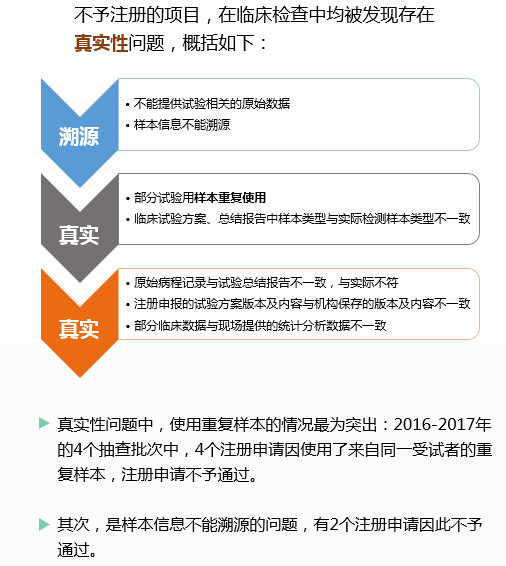
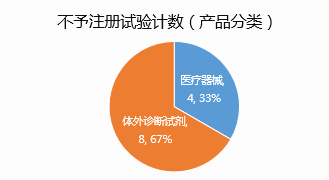
使用重复样本的情况多,2016至2017年的4个抽查批次中,共有4个注册申请因为使用了来自同一受试者的重复样本,注册申请不予通过。样本信息不能溯源的情况也较为突出,有2个注册申请因此不予通过。
2016年第98号通告的附件1分两个部分对医疗器械和体外诊断试剂临床试验现场检查要点提供了参考。本次征求意见稿除了按照时间变化更新了参考的法规之外,对于核查要点和检查结果判定原则给出了更为详细的描述,并且增加了对于检查方法的说明,反映了监管部门对于注册目的的临床试验管理要求越来越严格;同时,不管是对于医疗器械临床试验机构的临床试验管理部门在日常对本机构开展的临床试验进行监管、质控,还是申办者的临床试验日常操作、管理来说,都更具指导和参考意义。
征求意见已于6月30日截止,2018年第一批抽查名单已公布,奥咨达专家预测这一批次的注册申请将按照本次征求意见稿定稿后的细则进行。一般通告抽查名单后的两个月左右会公布抽查结果,让我们静静等待这次检查将对行业带来什么样的风向指导吧。
赶紧识别二维码进入阅读法规专刊第三期吧!

法规专刊第三期

医疗器械注册
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632