OLABS ∨
解决方案 ∨

▲
新年巨献
《2017年奥咨达医疗器械行业蓝皮书》
记录行业发展的足迹,
分享行业成长的动态,
展望行业前进的方向!
为全面回顾和分析2017年中国医疗器械产业发展状况,奥咨达医疗器械服务集团特组织了资深行业专家编写了《2017奥咨达医疗器械行业蓝皮书》,为读者们全面梳理2017年医疗器械行业的监管法规、重大事件、资本动态以及分享奥咨达对未来发展趋势的展望。全书分为六部分:医疗器械行业发展概况、中国医疗器械行业监管情况、注册评审情况、行业投融资概况、2017年产业发展回顾以及行业未来十年发展预测。通过详实的资料、数据、图表进行客观的分析论述,全面反映了医疗器械行业发展现状,展望行业未来发展方向,是行业内不可多得的参考资料。
重点新法规的介绍和影响分析
(一)关于深化审评审批制度改革鼓励药品医疗器械创新的意见
根据习近平总书记对食品药品监管提出的“四个严”重要指示和李克强总理提出的“深化药品医疗器械审评审批制度改革”的要求,国家食品药品监督管理总局加快了改革药品医疗器械审评审批制度改革步伐。2017年10月8日,中共中央办公厅、国务院办公厅印发了《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》,这是继2015年8月《国务院关于改革药品医疗器械审评审批制度的意见》之后,又一个深化药品医疗器械审评审批制度改革的纲领性文件,对我国医药产业创新发展具有里程碑意义。
表2-1 创新审评改革文件
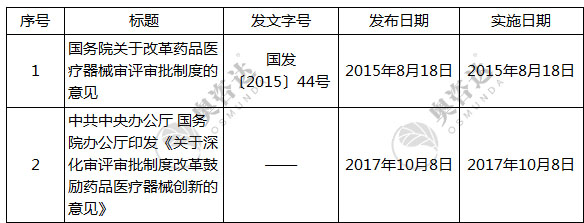
来源:NMPA官网
《关于深化审评审批制度改革鼓励药品医疗器械创新的意见》(以下简称“意见”)的出台是针对当前药品医疗器械创新面临的突出问题,着眼长远制度建设。《意见》提出改革临床试验管理、加快上市审评审批、促进药品医疗器械创新和仿制药发展、加强药品医疗器械全生命周期管理、提升技术支撑能力、加强组织实施6部分共36项改革措施。重点包括:扩充临床试验资源、接受企业在境外取得的临床试验数据、优化药品医疗器械上市流程、强化知识产权保护、加快推进仿制药质量和疗效一致性评价等10项具体任务。
《意见》主要围绕“创新”与“质量”两个关键词展开。目前,我国无论是创新能力、药械质量还是可及性,都与世界第二大经济体的地位不相符。《意见》的及时出台,对中国医药行业与国际接轨将起到非常关键的推动作用。其中,《意见》中有许多鼓励创新的政策条款,呼应了业界多年以来的期待。比如对知识产权的保护政策,包括建立药品专利链接制度,开展药品专利期限补偿制度试点,完善和落实药品试验数据保护制度等,都是构建医药创新型国家的配套政策。同时,《意见》提出的各相关部门要协调配合、形成改革合力,是该文件的一大亮点。药品和医疗器械创新工程浩大,《意见》指出,国家食品药品监管部门应发挥牵头作用,抓好改革具体实施,协调推进任务落实。而各相关部门包括发展改革部门、工信部门、科技部门、卫生计生部门等要分工协作,形成改革合力。对比以往政策,这是首次将各部委的角色定位与职责罗列清晰的文件,为后续政策的有力、有序实施提供了重要保障。
《意见》由中共中央办公厅、国务院办公厅发布,力度前所未有,不仅对创新企业是极大的鼓舞,而且对保证用械安全带来了积极正面的影响,引起医药行业内的广泛关注。业内人士称这份文件是中国医药行业迎来的建国后重大政策,对于促进药品医疗器械产业结构调整和技术创新,提高产业竞争力,满足公众临床需要都有指导性意义。
《意见》的出台,阐明了药品医疗器械监管的一系列重要理念,指出了审评审批制度改革的基本方向,明确了鼓励创新的重大政策,提出了加强能力建设的重要任务。对于促进药品医疗器械产业结构调整和技术创新,提高产业竞争力,满足公众临床需要,终促进医药产业健康发展具有里程碑意义。相信2018年,一系列配套落实的规章文件将会陆续出台[9]。
(二)医疗器械监督管理条例的修订
《医疗器械监督管理条例》(以下简称为《条例》)是为了保证医疗器械的安全、有效,保障人体健康和生命安全制定。于2014年2月12日国务院第39次常务会议修订通过,由国务院于2014年3月7日发布,自2014年6月1日起施行。
......
以上为部分内容节选,详见
《2017奥咨达医疗器械行业蓝皮书》
为全面回顾和分析2017年中国医疗器械产业发展状况,奥咨达医疗器械服务集团特组织了资深行业专家编写了《2017奥咨达医疗器械行业蓝皮书》,为读者们全面梳理2017年医疗器械行业的监管法规、重大事件、资本动态以及分享奥咨达对未来发展趋势的展望。全书分为六部分:医疗器械行业发展概况、中国医疗器械行业监管情况、注册评审情况、行业投融资概况、2017年产业发展回顾以及行业未来十年发展预测。通过详实的资料、数据、图表进行客观的分析论述,全面反映了医疗器械行业发展现状,展望行业未来发展方向,是行业内不可多得的参考资料。

目录
第一部分 2017年医疗器械行业发展概况
▶ 一、中国医疗器械行业政策法规动态
(一)国务院
(二)其他部委
(三)国家食品药品监督管理总局
(四)各省市药监局发布法规文件
▶ 二、医疗器械行业政策法规动态
(一)美国新法规及唯一医疗器械标识制度动态
(二)欧盟新法规动态
(三)国际标准动态
▶ 三、中国医疗器械行业市场发展状况
(一)行业总体发展概况
(二)热门细分领域发展概况
(三)行业产销情况分析
(四)全国不同区域医疗机构情况
▶ 四、医疗器械行业市场发展状
(一)行业总体发展概况
(二)细分领域发展概况
(三)医疗器械企业20强概况
(四)世界主要地区医疗器械行业运行情况
第二部分 2017年中国医疗器械行业监管情况
▶ 一、重点新法规的介绍和影响分析
(一)关于深化审评审批制度改革鼓励药品医疗器械创新的意见
(二)医疗器械监督管理条例的修订
(三)造假入刑
(四) 新版医疗器械分类目录
(五)临床豁免目录
(六)医疗器械注册人制度
(七)独立第三方医疗机构
(八)全生命周期监管
(九)临床机构备案制
(十)境外飞检
▶ 二、行业运行监管状况
(一)临床试验核查情况
(二)GMP飞检情况
(三)经营飞检情况
(四)医疗器械质量公告
(五)医疗器械召回情况
第三部分 中国医疗器械注册相关情况
▶ 一、2017年中国医疗器械注册审批产品情况
(一)国家局注册审批情况
(二)各省市注册审批情况
(三)2015-2017年医疗器械注册审批情况
▶ 二、2017年各国医疗器械注册收费概况
(一)美国FDA医疗器械注册收费标准
(二)加拿大HC医疗器械注册收费标准
(三)欧盟CE认证费用
(四)中国医疗器械注册行政收费概况
▶ 三、2017年医疗器械退审产品概况
(一)2017年NMPA不予注册情况
(二)2014年-2017年不予注册情况汇总
(三)2014-2017年退审情况分析
▶ 四、2017年创新医疗器械审批公示汇总
(一) NMPA发布创新审批相关法规文件
(二)NMPA医疗器械创新公告
(三)各省市药监局医疗器械创新公告
▶ 五、医疗器械优先审批情况
(一)医疗器械优先/快速审批相关法规文件
(二)NMPA医疗器械优先公告
(三)各省市医疗器械优先公告
(四)各省市医疗器械快速审批公告
未完待续...
▼
电子版:38元
★★★★★

长按识别二维码
数量有限,欲购从速!
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632