OLABS ∨
解决方案 ∨
近期,上海市药监局在上海医疗器械注册人制度试点工作经验分享中指出,自医疗器械注册人试点推出以来,实践中存在着一些问题,需要注册人和受托企业高度重视:
医疗器械注册人、受托企业的权责落实不到位。
部分试点企业对委托生产质量协议和受托生产质量管理体系要求理解不到位,导致双方责任分工不够清晰。尤其是注册人与受托企业在技术文件转移、生产放行、上市放行等关键环节责任分配不清、流于形式,致使管理制度的执行衔接不畅,对产品质量安全带来风险隐患。
跨省衔接还需进一步加强。注册人和受托企业现场核查协同需加强。
由于尚未建立全国统一的信息平台,只能依靠发函的方式建立联合检查机制,检查信息互通的滞后问题时有发生。
知识产权保护风险需高度关注。
在试点期间,上海市药监局在注册审评环节曾发现,位于本市的A注册申请人与本市的B受托生产企业签订委托生产协议,但由于A忽视了知识产权保护的相关内容,出现B擅自利用A的研发资料,另行提出注册申请的情形。

医疗器械委托生产,找奥咨达。2018年4月,为承接医疗器械注册人制度,助力创新转化,打造医疗器械产业生态圈,奥咨达全球产业模式“Cloud医械云 + CDMO研发制造 + CRO 高端服务” - 医疗器械3C产业平台诞生!依托于奥咨达集团强大资源和优质项目经验,将智能制造与高端服务双业融合,通过“医疗器械+互联网+高端服务+先进智造”服务模式,为医疗器械企业提供全产业链的一站式解决方案,很好的规避了上述风险。
目前, 奥咨达集团第一期已建成超过32000平的厂房与实验室,包含长三角的上海科创中心8000㎡,珠三角的深圳科创中心 4000㎡,江西上饶产业园20000 ㎡,可覆盖I/II/III类有源、无源、IVD以及高风险植入类医疗器械,第二期,第三期规划已于2020年开始,两年内将建成超过700亩的3C产业基地。
奥咨达CDMO平台自运营以来,已孵化40多个项目,并率先取得国内首张第三方服务平台的注册证。

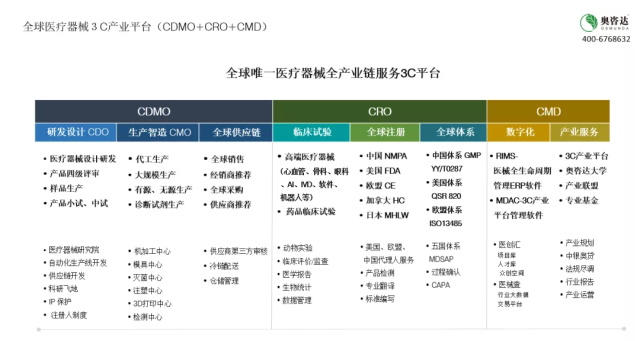
奥咨达CDMO平台提供概念创意孵化、专利技术购买、设计研发与转化、样品生产、批量代工、定制化生产、厂房租赁、产线转移、行业资源对接、政策解读与指导以及GMP、ISO13485生产方案等涵盖CRO(临床注册)、CDO(设计研发)、CMO(生产制造)三大模块的服务,且合作模式灵活,如客户可选择CRO或CRO+CMO或CDO+CRO+CMO;针对不同需求,奥咨达CDMO提供定制化服务;对于需要集中生产的快速转移企业,可提供委托生产及注册申报服务;对于有新产品需要注册的生产企业,可供检验检测、临床试验、注册申报、委托生产等服务;对于科研机构、创新企业、渠道商转型企业,可提供产品研发等全产业链、一站式全流程服务,将您的医学科研成果快速实现临床应用并产业化。
医疗器械委托生产 找奥咨达 400-6768632
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632