OLABS ∨
解决方案 ∨
9月14日,北京市药品监督管理局召开北京市医疗器械临床试验监督抽查工作动员部署会,重点对北京市2020年医疗器械临床试验监督抽查工作进行部署,并对各检查组进行医疗器械临床试验检查培训,明确检查要求,统一检查标准。
此次监督抽查工作根据本市医疗器械临床试验备案信息,依据《医疗器械临床试验质量管理规范》、《医疗器械临床试验检查要点及判定原则》、《体外诊断试剂临床试验现场检查要点及判定原则》、《医疗器械临床试验机构条件和备案管理办法》、《北京市临床试验用医疗器械管理指南》等文件,对8个已备案的临床试验项目的真实性、合规性实施检查,产品涵盖了境内第二类有源、无源、体外诊断试剂和创新医疗器械等产品。医疗器械临床试验监督抽查项目通告已在官方网站发布。
开展医疗器械临床试验监督抽查工作将进一步加强北京市医疗器械临床试验监督管理,规范医疗器械临床试验工作,强化申办方和临床试验机构的法律意识、诚信意识、责任意识。对监督抽查发现的问题,北京市药品监督管理局将依据相关法律法规进行处理,监督抽查情况和处理结果将面向社会公布。
2020年医疗器械临床试验监督抽查项目
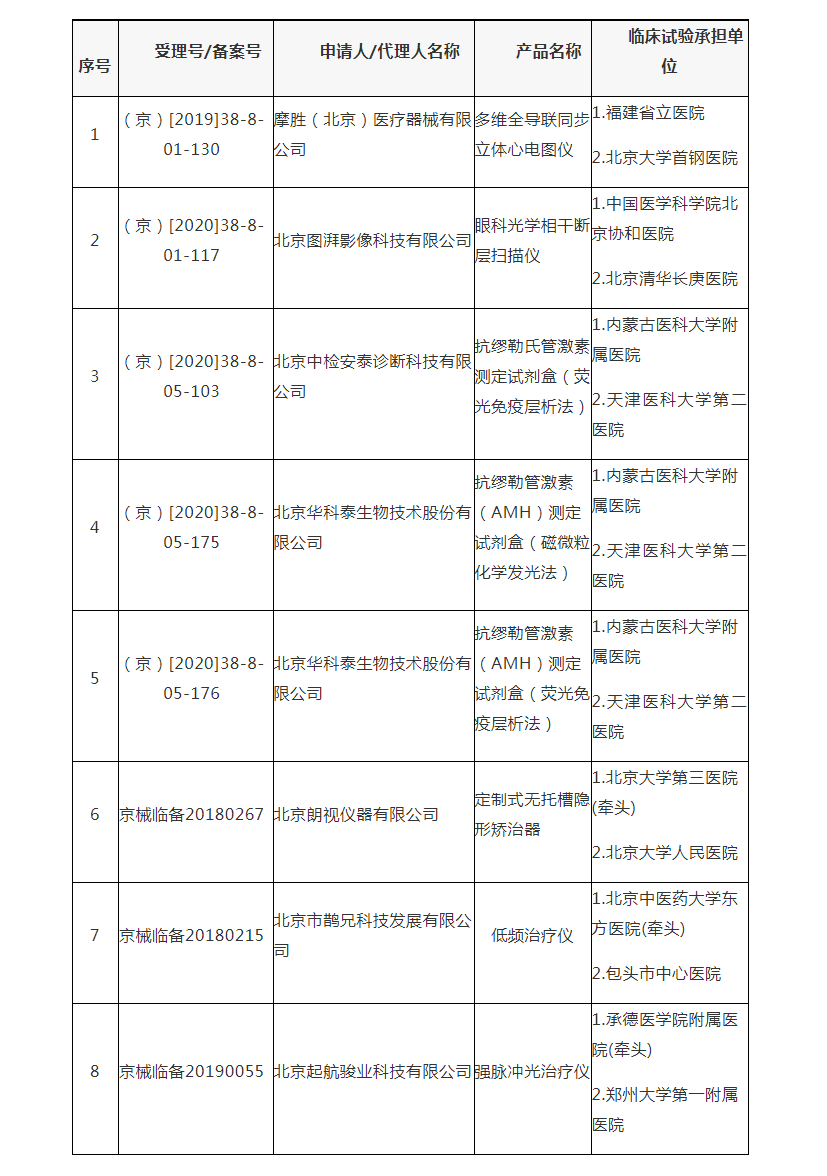
【文章来源】北京药监局
【全文整理】奥咨达 奥咨达是一家全球性医疗器械3C认证平台,提供医疗器械注册、医疗器械临床、医疗器械认证等一站式服务。
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632