OLABS ∨
解决方案 ∨
国家药监局综合司关于印发医疗器械生产质量管理规范独立软件现场检查指导原则的通知
为加强医疗器械生产企业实施《医疗器械生产质量管理规范》及其附录独立软件的监督检查,指导监管部门开展现场检查和检查结果评估,国家药监局组织制定了《医疗器械生产质量管理规范独立软件现场检查指导原则》。现印发给你们,请遵照执行。
国家药监局综合司
2020年5月29日
附件


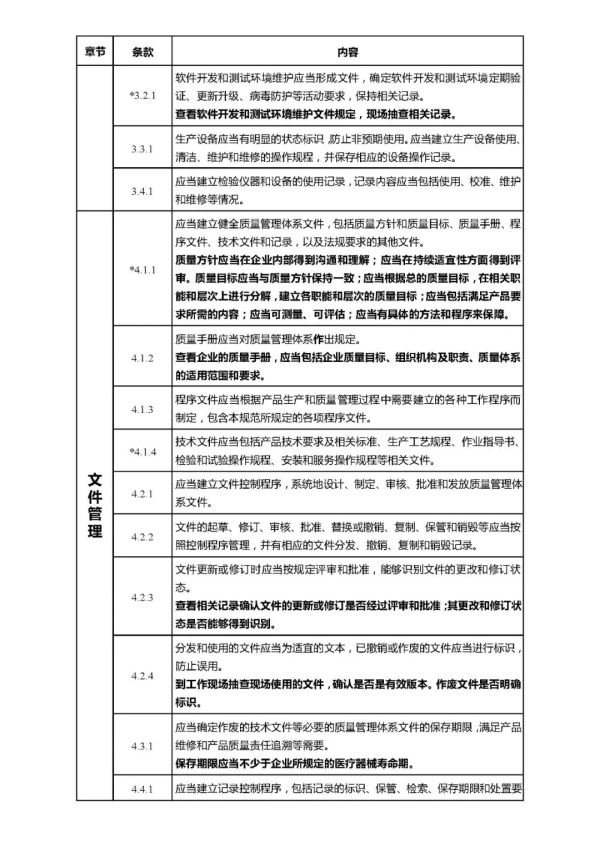
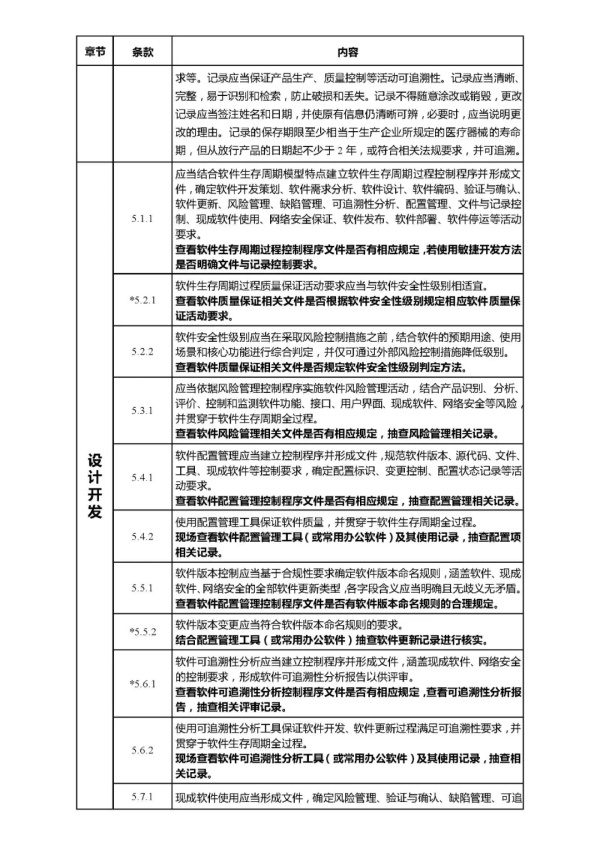






文章来源于国家药监局,全文由奥咨达整理。了解更多关于医疗器械注册、医疗器械生产的政策法规,请关注奥咨达动态。
如果你有寻找医疗器械孵化,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632
您想参观OLABS创新工厂,
那就与我们取得联系吧!
您可以填写右边的表格,让我们了解您的服务需求,这是一个良好的开始,我们将会尽快与你取得联系。当然也欢迎您给我们写信或是打电话,让我们听到你的声音!
24小时免费咨询热线:
400-6768632